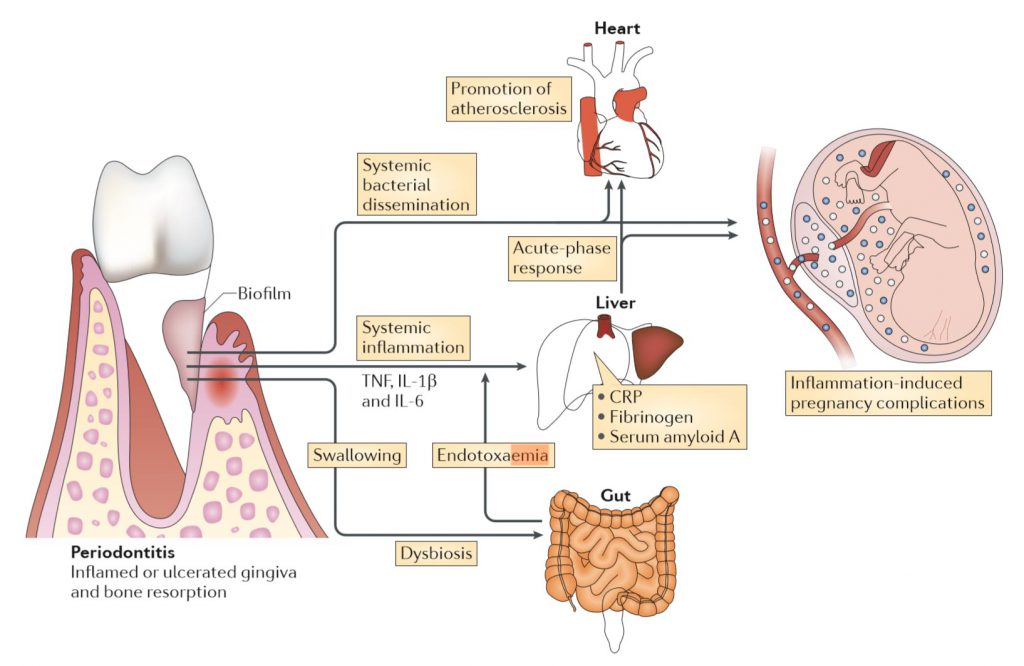
Biologically plausible mechanisms linking periodontitis to systemic inflammation and disease
De très nombreuses études suggèrent que les maladies parodontales – en particulier la parodontite – sont étroitement liées à l’athérothrombose, mais il n’existe aucune preuve démontrant que ce lien est causal (Lockhart et al. Circulation 2012: 125; 2520-2544). La parodontite est traitable et peut être évitée par l’hygiène bucco-dentaire et les soins bucco-dentaires professionnels. Une fois établie, la parodontite est traitée par l’élimination des infections dans les poches parodontales.
Le lien entre la parodontite et l’athérothrombose est étayé par des études in vitro, animales et cliniques. La parodontite est responsable de la perte d’attache gingivale autour des dents, et conduit à la formation d’une « poche parodontale », qui agit comme un réservoir pour les pathogènes parodontaux. Les bactéries parodontales et / ou leurs produits inclus dans un biofilm sous-gingival pénètrent fréquemment dans la circulation sanguine via la partie interne de la poche parodontale ulcéreuse. Du fait de leur tropisme pour la fibrine et pour d’autres molécules de la matrice extracellulaire, les bactéries buccales dans la circulation peuvent adhérer aux sites de lésion artérielle, dans tout le système cardiovasculaire. Les bactéries peuvent exercer une action pathogène soit directement, en libérant par exemple des protéases spécifiques telles que les gingipaïnes de Porphyromonas gingivalis – un pathogène parodontal majeur – ou indirectement en stimulant une réponse inflammatoire locale et/ou systémique (Nat Rev Immunol., 2015, 15: 30-44).
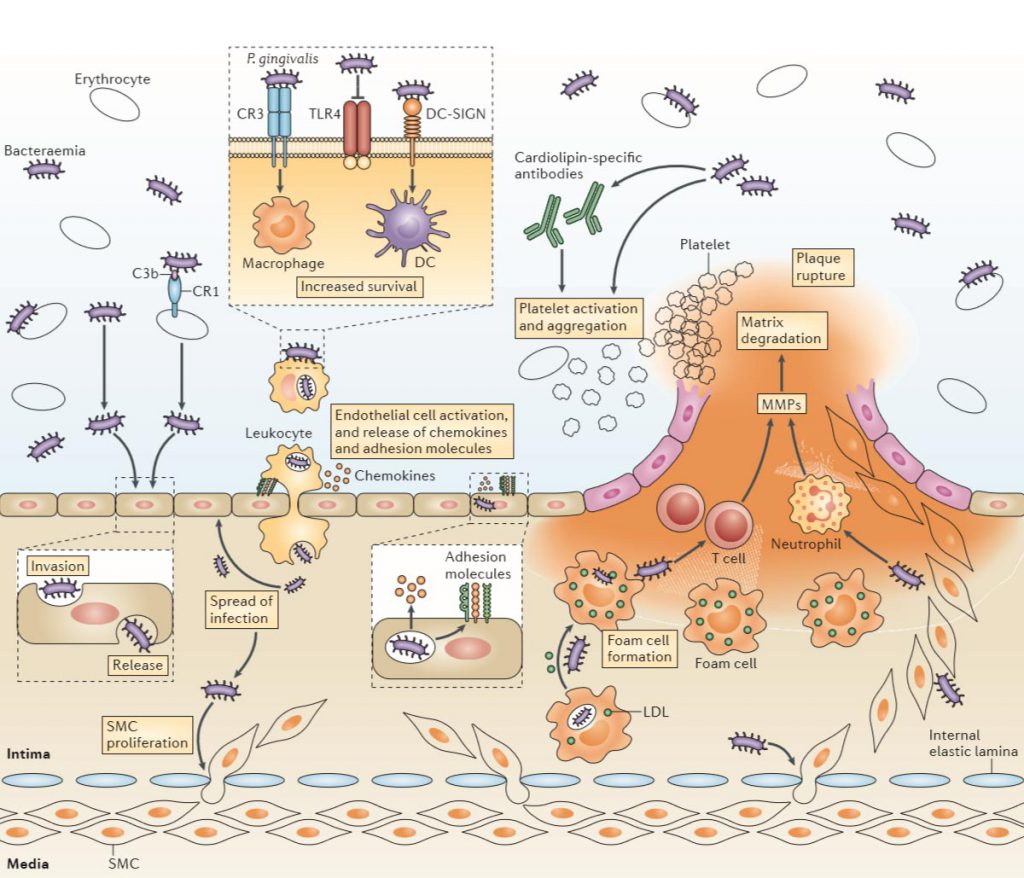
Microbial immune subversion in atherogenesis
Une corrélation entre le microbiote sous-gingival et les pathogènes détectés dans les lésions vasculaires a été démontrée. Ainsi, bien que les mécanismes pathogènes qui relient les maladies parodontales à l’athérothrombose restent peu clairs, l’association biologique entre les deux conditions est claire. Il est nécessaire d’évaluer le rôle causal de la pathologie parodontale par des études d’intervention. Nous ne disposons actuellement d’aucune preuve montrant le bénéfice du traitement parodontal dans la prévention des événements cardiovasculaires. Des études utilisant la CRP ou la fonction endothéliale comme paramètres d’évaluation du bénéfice ont suggéré une amélioration après la thérapie parodontale (D’Aiuto et al. J Clin Periodontol 2013;40-Suppl.14:S85–S105).
Malheureusement, les études d’intervention visant à améliorer l’hygiène bucco-dentaire dans la prévention des maladies cardiovasculaires chez les sujets atteints de parodontopathie vont exiger un recrutement de patients très important et une longue période d’observation. Nous avons choisi d’évaluer le rôle de la parodontite dans l’initiation et la progression de la maladie athérothrombotique en utilisant l’imagerie moléculaire des plaques athéromateuses comme marqueur intermédiaire de la maladie. De plus, le statut biologique parodontal sera évalué et suivi par une analyse combinée des communautés microbiennes et des effecteurs immuns de l’hôte. Une telle approche combinée des biomarqueurs a récemment été utilisée dans les échantillons de salive de patients atteints de coronaropathie (J Clin Periodontol 2014; 41: 442-450). En étudiant les communautés microbiennes et les effecteurs immunitaires de l’hôte dans les échantillons créviculaires gingivaux, nos études pourraient fournir des résultats plus fiables et plus robustes sur l’état de santé parodontale.
